(一) 围骨折期管理
1.提高围骨折期骨质疏松症的诊断率
加强医务工作者对骨质疏松症防治的关注程度,提高骨质疏松症的诊断率,是骨质疏松症防治的第一步。有骨质疏松危险因素的人群应及早进行骨质疏松症筛查,骨质疏松症的诊断需结合患者的年龄、性别、脆性骨折史、临床风险因素以及骨密度检测结果等进行综合分析,2014 年的美国国家骨质疏松基金会(National Osteoporosis Foundation,NOF) 骨质疏松诊疗指南推荐,建议50 岁以上有骨折的人群进行骨密度检查,50 ~64 岁绝经女性及50 ~69 岁男性伴脆性骨折者行腰椎影像检查。
需要指出的是,原发性骨质疏松性骨折的诊断应注意与继发性骨质疏松导致的骨折进行鉴别,继发性骨质疏松的病因很多,主要包括骨转移瘤、多发性骨髓瘤等骨肿瘤,甲状旁腺功能亢进症、甲状腺功能亢进和性激素缺乏等内分泌代谢疾病,其他系统性疾病,药物性骨质疏松症。继发性骨质疏松症可发生于各年龄段,除有骨质疏松症的表现外,往往有原发病的临床表现和实验室检查异常,其骨质疏松的严重程度往往与原发疾病相关,当原发病治愈或缓解后,骨质疏松通常会好转。
2.围骨折期治疗方案
骨质疏松性骨折的治疗有别于一般的外伤性骨折,骨质疏松性骨折围骨折期除进行常规的外科治疗外,需要同时缓解疼痛,减少患者的制动时间,抑制快速骨丢失,提高骨强度,并积极治疗骨质疏松症,预防再发骨折。
(1) 骨折术后疼痛及骨丢失管理: 由于患者在骨折围骨折期需要制动,增加了废用性骨质疏松的危险,其严重程度取决于制动的时间和方式,骨折急性期患者制动后每周的骨丢失量约占骨总量的1%,相当于正常人1 年的“ 生理性骨丢失量”,2 周内每24 小时的尿钙排出量增加40% 。而骨折后患者因疼痛导致制动时间延长,将进一步加重骨丢失。因此骨折后需要迅速有效地止痛,尽快恢复患者活动能力,避免由于长时间制动而造成持续性骨丢失。
(2) 抗骨质疏松药物治疗:骨折手术使用接板和螺钉固定后可能会出现局部“应力遮挡” 效应及内外骨膜血管的损伤,在接板下可发生局部骨质疏松,导致局部快速骨丢失 。同时,患者的骨质量对于手术成功与否至关重要: 骨质疏松会加大手术复位的难度,导致内固定物的稳定性差,内固定物及植入物易松动或脱出。由此可见,骨质疏松围骨折期应进行积极的抗骨质疏松药物治疗,改善骨质量,提高骨强度,避免患者陷入骨折-快速骨丢失-再骨折的恶性循环中。
抗骨质疏松药物有很多种,作用机制也各异,主要包括以抑制骨吸收为主,或以促进骨形成为主,以及一些具有多重作用机制的药物,国内已批准上市的抗骨质疏松药物及药物作用。
(二) 长期抗骨质疏松管理
1.长期抗骨质疏松治疗目的
骨质疏松性骨折手术治疗后,如不进行持续的抗骨质疏松治疗,骨丢失会更加严重,进一步加重骨质疏松,易发生骨折延迟愈合或不愈合,并易造成内固定松动、假体脱出等不良后果,且再发骨折风险明显增高。最终导致致残率、致死率增高,因此,抗骨质疏松治疗是持久的任务,必须重视长期的抗骨质疏松治疗,提高患者的依从性,预防再骨折的发生。
2.治疗方案
(1) 基础措施:
调整生活方式: 除遵循一般的术后康复规律,如功能锻炼,还需要坚持健康的生活方式,如摄入富含维生素D、钙、低钠和适量蛋白质的均衡膳食,避免嗜烟、酗酒,慎用影响骨代谢的药物等。
补充钙剂和维生素D: 同时补充钙剂和维生素D 可降低骨质疏松性骨折风险[18] 。摄入适量钙剂可减缓骨量丢失,改善骨矿化。用于治疗骨质疏松症时,钙剂应与其他抗骨质疏松药物联合使用。补充适量维生素D 以增进胃肠道的钙吸收,促进骨基质矿化,活性维生素D 可增强肌肉力量,改善神经肌肉协调及平衡能力。中国大陆地区7 个省份的调查报告显示,我国55 岁以上女性血清总钙质量浓度平均值为2.32 mmol/L (9.3 mg/dL),25羟维生素D 质量浓度平均值为18.0 ng/mL,61.0%的绝经后女性存在维生素D 缺乏[19] 。建议老年人根据自身钙和维生素D 的摄入水平适当补充,目前我国营养学会推荐,如果饮食中钙供给不足可选用钙剂补充,绝经后妇女和老年人钙摄入推荐量为1 000 mg/d,维生素D 推荐剂量为400 ~800 IU/d。
预防跌倒: 大多数骨质疏松性骨折与跌倒有关,老年人应注意加强自我保护,注意防治增加跌倒风险的疾病,避免使用影响机体平衡的药物[20] 。肌少症是老年人中常见的一种以骨骼-肌肉量下降、肌力减退为主要特征的综合征,患有肌少症的患者容易发生跌倒,增加再骨折风险。适当进行运动锻炼,增强肌肉力量,同时预防和延缓肌少症的发生是预防再骨折的重要措施。
(2) 提高抗骨质疏松药物治疗的依从性:
抗骨质疏松药物治疗过程中患者的依从性至关重要,良好的依从性是保证抗骨质疏松药物疗效的前提.研究数据提示,漏服一半剂量的抗骨质疏松药物,会减少90%以上的骨保护效果。然而,在抗骨质疏松治疗的临床实践中,患者的依从性并不乐观; 有数据显示,坚持抗骨质疏松治疗的依从性在第6、12 和24 个月分别为70%、59%和4% 。外科与内科之间的转诊有助于提高骨质疏松药物治疗的依从性,国内已有部分医院在院内探索性地建立了骨质疏松患者在外科与内科之间转诊、衔接临床诊疗路径,但是骨科医生并不能轻视骨质疏松治疗的责任。目前,我国亟须建立、完善和推广此类临床路径,同时在公众和医疗界中强化抗骨质疏松治疗依从性的重要性认识。
(三) 抗骨质疏松治疗疗效评价
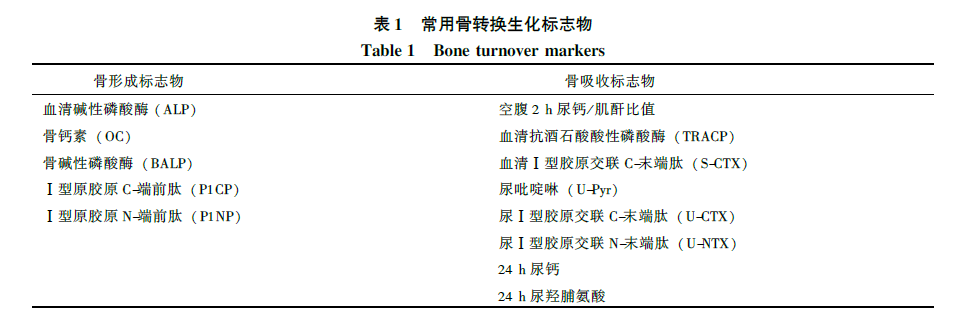
抗骨质疏松治疗效果的骨密度评价需要较长周期,而早期可通过观察骨转换生化标志物了解药物的作用效果,预测疗效,增加用药的依从性。通常,应以术后或药物治疗前检测作为基线值,药物治疗3 ~6 个月后可能测得骨转换生化标志物的变化,但不能根据变化的绝对值而是依据最小有意义变化值(least significant change,LSC) 进行判断。常用骨转换生化标志物。
在以上指标中,IOF 推荐血清Ⅰ型原胶原N-端前肽( serum procollagen type 1 N propeptide,P1NP) 和血清Ⅰ型胶原交联C-末端肽(serum Cterminal telopeptide of type Ⅰ collagen,S-CTX) 是敏感性相对较好的骨转换生化标志物 。在开始抗骨质疏松治疗后的1 ~2 年进行一次骨密度(bone mineral density,BMD) 检查,随后每2 年监测一次 ,以评价药物治疗的长期疗效。由于测量仪器、部位及测量技术等差异,进行疗效评价时,同样应充分考虑骨密度的最小有意义变化值,如何评价和计算LSC,可以参考国际临床骨密度测量协会网站 。需注意的是,外周骨骼骨密度或骨矿含量检测不能反映脊柱及髋部对于药物治疗的反应,因此不适于评价药物疗效。
每年进行身高测量,当身高降低超过2 cm 时应进行腰椎影像检查,以确定是否有新发的椎体骨折。在3 ~5 年治疗期后,基于以上指标,需要进行全面骨折风险及抗骨质疏松治疗效果评估。




